化学反応式はHCl NH3 → NH4Cl となり塩化アンモニウムが生成されます。 本来なら酸のH と 塩基の OHが反応をして水を生成するのですが、アンモニアにはOHがないので、 NH3自身がHを受け取ってアンモニウムイオンNH4となり、それが残りの陰イオンと化学名 アンモニア水(水酸化アンモニウム) 化学式 NH 4 OH 英語名 ammonia solution, ammonia water, ammonium hydroxide アンモニア水の特徴 アンモニアガスの水溶液で、薬局で市販されているものは10%溶液です。比較的手軽に入手できます。 やや強いアルカリ性を示します。 急いでいる人のために、まずは アンモニアの性質のまとめ を書いておくね。 アンモニア (化学式NH3)の性質まとめ 作り方 ①水酸化ナトリウム+塩化アンモニウム (+水) ②水酸化カルシウム+塩化アンモニウム (加熱) ③アンモニア水を加熱 集め方 上方置換法 色

アンモニア水とテトラアンミン亜鉛 の化学式についてですが なぜアンモニアは4mo Clear
アンモニア水 化学式 電離
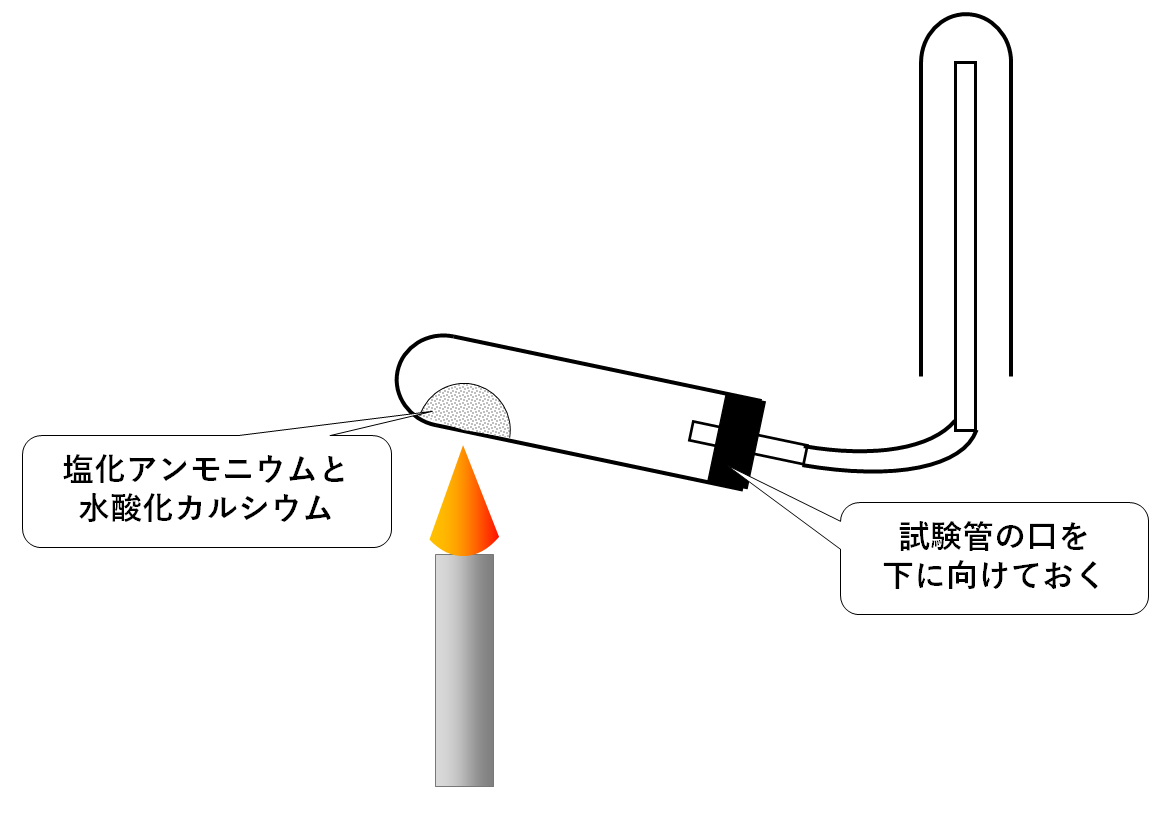
アンモニア水 化学式 電離-ここでHは アンモニア水 系のヘンリー定数である このときの水蒸気圧をPと すれば,気 相のアンモニア と水のモル分率ma,mwは それぞれ次の式で表わさ れる (2) 水とアンモニアの分子量はそれぞれお よび で あり,海 水淡水化などで扱うアンモニアの 化学反応式 2NH 4 Cl Ca(OH) 2 → CaCl 2 + 2H 2 O 2 NH 3 (塩化アンモニウム 水酸化カルシウム→ 水 + 酸素) アンモニアは、 ・水に 非 常に溶けやすく、 空気よりも軽いため 上方置換法 で集める。 ・ 水に溶けると アルカリ性 を示す。 ・刺激臭がある。



アンモニアと硫酸の中和の化学反応式の書き方か分かりません 途 Yahoo 知恵袋
1906 年にドイツでハーバーとボッシュがアンモニアの合成に成功した。この方法は,水と石炭と空気からパ ンを作る方法とも言われ,窒素の化学肥料の誕生により農作物の収穫量は飛躍的に増加し世界を飢餓から救った と言われている。なお、水溶液中では、水 h 2 o が配位しているのが当然であるから、アクア錯イオンなどを表記するときは、水 h 2 o を省略して反応式を書くことも多いです。次に、水 h 2 o 以外が配位している代表的な錯イオンを示します。 (i) 配位子がアンモニア nh 3 の第62章 水溶液中のイオンの反応 08ko062 水溶液中に,ある金属の陽イオンが溶けています。 さて,そのイオンが何かを知るには,どうすればよいでしょうか。 この章の学習内容は,次の通りです。 (1) 塩化物イオン (2) 硫化物イオン (3) 水酸化物
化学名又は一般名 アンモニア水 (Aqua ammonia) (aqeuous ammonia) 別名 水酸化アンモニム (Ammonium hydroxide) 濃度又は濃度範囲 100% 分子式 (分子量) NH4OH (351) 化学特性 (示性式又は構造式) CAS番号 官報公示整理番号(化審法) (1)314 官報公示整理番号(安衛製品名 (化学名・商品名等) : アンモニア水 2%のホウ酸水で鼻と喉を洗浄する。 呼吸困難の場合は酸素吸入を行い、速やかに医師の診断を受ける 速やかに容器を安全な場所に移す。 移動不可能の場合は、容器及び周囲に散水して冷却する 漏洩箇所を硝酸 Wikipedia 特性 化学式 HNO 3 精密質量 g mol1 外観 無色の液体 密度 g cm3 融点416 C, 232 K, 43 F 沸点 6 C, 356 K, 181 F (68 % 溶液は 121 C で沸騰) 水への溶解度 完全に溶解 酸解離定数 pK a 各種金属イオンに少量のアンモニア水を加えてみた Duration 117
アンモニア水28% (NH 3) 和別名1 (水酸化アンモニウム) 和別名6 アンモニアスイ CAS RN ® メーカー名 キシダ化学沈殿の化学式 沈殿の色 光による変化 アンモニア水 チオ硫酸ナトリウム AgNO 3 +KCl AgNO 3 +KBr AgNO 3 +KIアンモニア水化学式, アンモニア水(28%) (アンモニア水(28%) Ammonia solution 28% 品番 (SDS) CAS No メーカー名—規格・用途 化学兵器 消防法 容量・単位 500ml 価格(本体) ¥ 2,600 メモ 検索ページに戻る 試薬のご購入とご使用に際して




水素水アンモニア暗い青色の背景上でのメタンの化学式と分子モデル アイコンのベクターアート素材や画像を多数ご用意 Istock
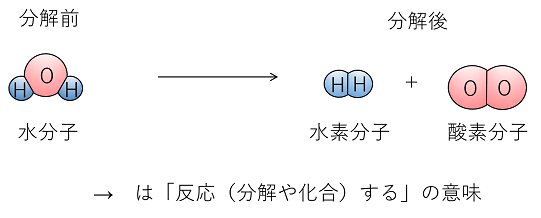



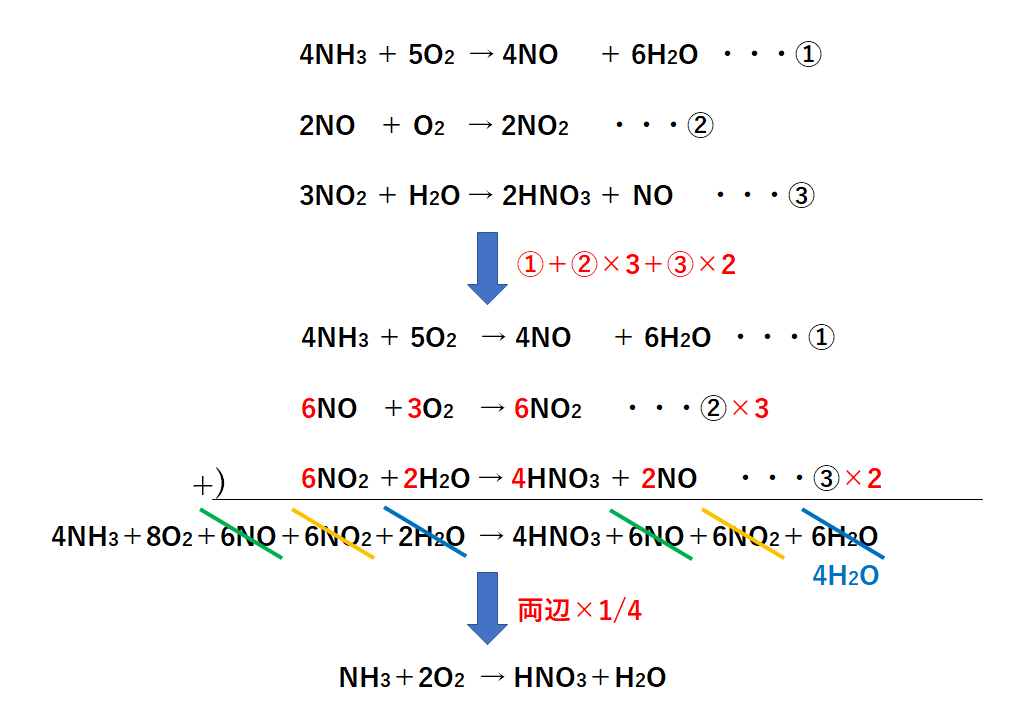
化学反応式
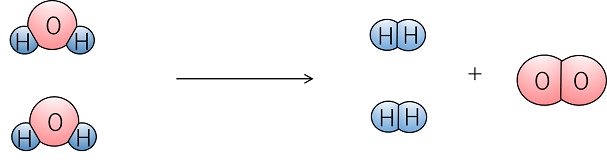
化学反応式の書き方 例1 水素の燃焼・・・水素+酸素→水 化学式・・・水素 (H2),酸素 (O2),水 (H2O) まず、水素+酸素→水をモデルと化学式で表す 両辺原子の数を数える 左辺のOが2個、右辺が1個なので右辺の水分子を増やす 右辺の物質は水なので、酸素硝酸アルミニウム水溶液にアンモニア水を少量滴下すると白色の水酸化アルミニウムが沈殿する。 解答 Al 3+ +3NH 3 +3H 2 O→Al(OH) 3 ↓+3NH 4 + アンモニア水もNH3ですが、水と反応するので、 NH3 + H2O → NH4OH となります。 さらにこれが電離すると、 NH4OH → NH4 + OH になり、この時生じたOHによって、アルカリ性の性質を持ちます。




水素水アンモニアメタンの化学式と分子モデル化学学校ノートブック檻の中の紙のシート 3dのベクターアート素材や画像を多数ご用意 Istock
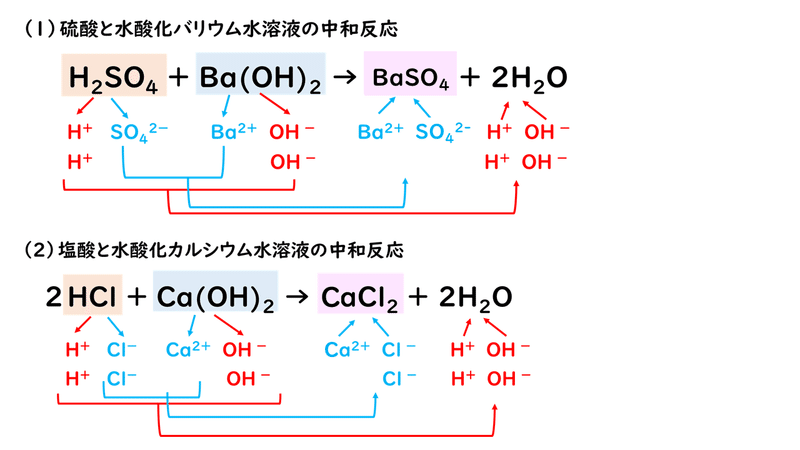



6 4 塩とその性質 おのれー Note
1概要と主な違い2アンモニアとは3水酸化アンモニウムとは4並列比較表形式のアンモニアと水酸化アンモニウム5概要 アンモニアとは? アンモニアは、化学式nh3のガス状物質です。 これは無機化合物であり、最も単純な水素化プニクトゲンでもあります。液化アンモニア(液安) アンモニア水(安水) 製品安全データ 組成・成分 化学特性(化学式または一般名) 官報公示整理番号(化審法・安衛法) cas № nh3 (1)ー391 7664ー41ー7 nh4oh (1)ー314 1336ー21ー6化学反応式 アンモニア 塩化アンモニウム+水酸化カルシウム →塩化カルシウム+アンモニア+水 2NH4Cl+Ca(OH)2 →CaCl2+2NH3+2H2O 塩素 さらし粉+塩酸→塩化カルシウム+塩素+水



アンモニアと硫酸の中和の化学反応式の書き方か分かりません 途 Yahoo 知恵袋




アクセス化学 例題解説 基本例題90 銅イオンの反応
銅アンモニア法人絹の酸化銅アンモニウム溶剤の調整剤 各種アンモニア錯塩の製造 メールフォーム 日化トレーディング株式会社 化学品部 化学品グループ TEL:02 FAX:02 東京営業所 TEL: FAX:アンモニア分子は、三角すい形 続いて、 アンモニア分子 です。 アンモニア分子は、3つの水素原子と1つの窒素原子からなっています。 こちらは少し複雑ですね。 このアンモニア分子は、窒素原子が上にあり、下の水素原子とくっついています。 このような形を、 「三角すい形」 といいます。 まずアンモニアだけど溶液中では水と反応して、 NH3→NH4 ()OH () となる! これを塩酸で中和すると、 NH4 ()OH ()HCl→NH4ClH2O となる! この生成物であるNH4Clは塩化アンモニウムと呼ばれるよ! 実果 2年以上前 ありがとうございます!



アンモニアと二酸化炭素の化学反応式の仕組みがわかりません 組み方 Yahoo 知恵袋



3
AgCl+ NH3 → ★塩化銀に過剰のアンモニア水を加える AgCl+2NH3→Ag(NH3)2++Cl- 塩化銀は過剰のアンモニア水を加えることでジアンミン銀イオンという錯イオンとなって溶解し無色の溶液になります。 アンモニア水 化学式について NH3 (アンモニア)H2O (水)=NH4OH (アンモニア水)またはアンモニア水 ③ヒートポンプ式蒸留法 - - 〇 - 〇 - アンモニアガス またはアンモニア水 ④ヒートポンプ式蒸留法 +H2 Harmony +燃料電池 - - 〇 ③の %減 - 〇 ③の %減 - 窒素ガスとして大気 放出 ⑤ヒートポンプ式蒸留法 +H2 Harmony



Q Tbn And9gctycc8q8jnbridwze1oqqfvz7qcuob8ywenf7z0cafriijjsdup Usqp Cau




化学工業の歴史1 無機 有機化学工業の基盤成立 化学工業の基礎知識2 ものづくり まちづくり Btob情報サイト Tech Note
便宜上,化学式は nh 4 oh と記述されるが,この式に相当する未解離の化合物は遊離の形で取出されていない。 アンモニア水中に存在するとされるが,アンモニア水のアルカリ性はアンモニア nh 3 の加水分解によって説明されるので,水酸化アンモニウムの存在を考える必要はない。アンモニア水中でのアンモニア分子の状態は、種々の実験事実から水酸化アンモニウムNH 4 OHの存在は考えられず、水分子の付加したNH 3 ・H 2 OとNH 4 OHの中間状態にあるものとされている。 アンモニアを水に溶かすと、以下の式のようになります。 NH3 h2o→nh4 oh そのため、アルカリ性になります。




1 2 Lihat Cara Penyelesaian Di Qanda
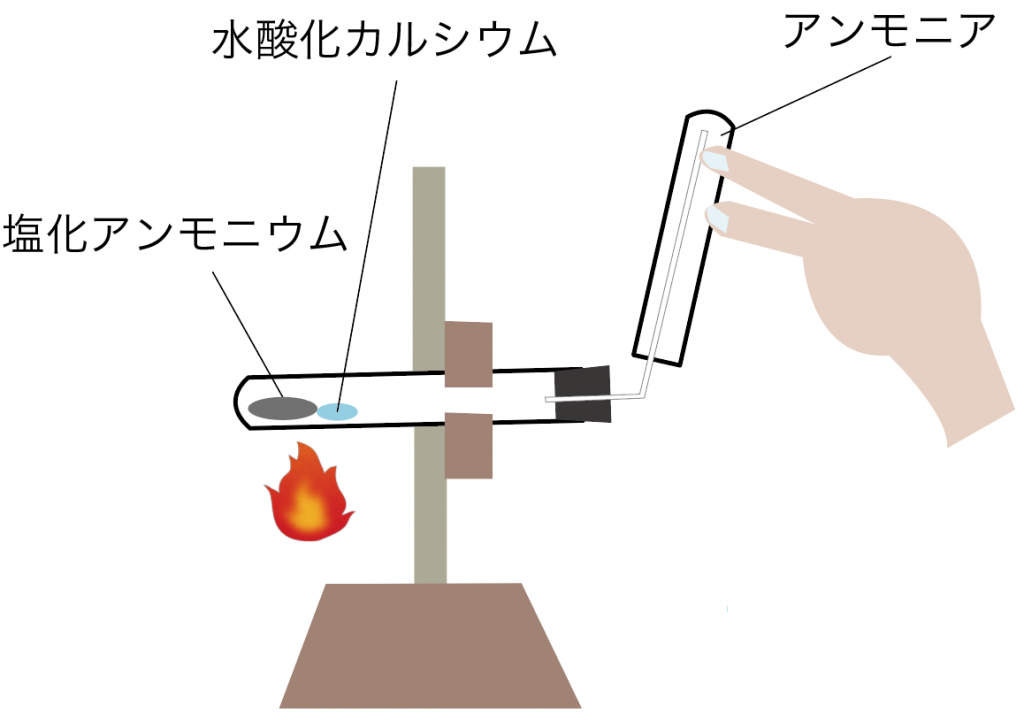



中1理科 3分でわかる アンモニアの発生方法 作り方 集め方 性質 Qikeru 学びを楽しくわかりやすく
鉛の化合物は水に溶けにくいものが多いが、硝酸鉛 Pb(NO 3) 2 や酢酸鉛 (CH 3 COO)Pb は水によく溶ける。 イオン 鉛(Ⅱ)イオン(Pb 2 )は様々な沈殿を作る。アンモニア水や少量の水酸化ナトリウム水溶液を加えると、水酸化鉛(Ⅱ)の白色沈殿を生じる。16.窒素と水素を化合させると,アンモニアが生成する。 N2 +3H2 →2NH3 17.硝酸銀水溶液に塩化ナトリウムを加えると,白い沈殿を生じる。 AgNO3 +NaCl →NaNO3 +AgCl理科で一次電池、二次電池を表す式を書いてきなさいと言われたんですが、教えていただけませんか🙇♀️ 中和反応で、酸性と石灰石が反応したときの化学反応式を知りたいです! 教えてください🙏 (1) (2) (3)の解き方がわかりません、 (1)は中和すると Ba (OH)2H2SO4→Baso42H2Oで水ができてイオンがなくなるから存在しないってことですか? 解説してほしいです。




17 号 アンモニア合成装置 Astamuse




アンモニア Wikipedia
佐藤禎一 栗田工業/KCRセンターの佐藤です。 №31の水処理教室では、「アンモニアを含んだ排水の処理」についてお話いたします。 アンモニアは富栄養化の原因となる窒素化合物です。 その濃度が高い場合や、排水量が多い時には生物学的処理方法が用いられます。 ここでは、排水量が少ない場合や濃度が極端に低い場合に用いられる物理・化学的処理について化学実験 (IV属 亜鉛) 石川 厚 硝酸亜鉛(II)水溶液にアンモニア水を加えれば水酸化亜鉛を沈殿し、アンモニア水の過剰量に溶ける。 アンモニア水 1滴 攪拌後 15Mのアンモニア水15滴 問題 3 以下の反応について,化学反応式を書け。 硝酸亜鉛(II)水溶液にアンモニア水を加えると水酸化亜鉛が沈殿する。化学式・化学反応式暗記プリント 水酸化バリウム+塩化アンモニウム→塩化バリウム+アンモニア+水 Ba(OH) 2 +2NH 4 Cl→BaCl 2 +2NH 3 +2H 2 O




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット




水と空気からアンモニア 100年続く製法超えられるか 朝日新聞デジタル
これは広い意味で化学反応と言えますから,溶解も熱化学方程式に含めます。 たとえば,塩化ナトリウムの水への溶解熱は39kJ /mol の吸熱です。 これを熱化学方程式で表すと,次式のようになります。①化学変化前の物質(反応物)を式の左側、化学変化してできた物質(生成物)を式の右側に書き、 左から右に矢印を書く(「=」でないので注意!)。 水素 + 酸素 → 水 ②物質を化学式で表し、矢印の左側と右側の原子の個数を数える。




なぜzn2 ではなくfe2 が沈殿したのでしょうか アンモニア水で沈殿す 化学 教えて Goo



Www Junsei Co Jp Product Search Sds jis Pdf
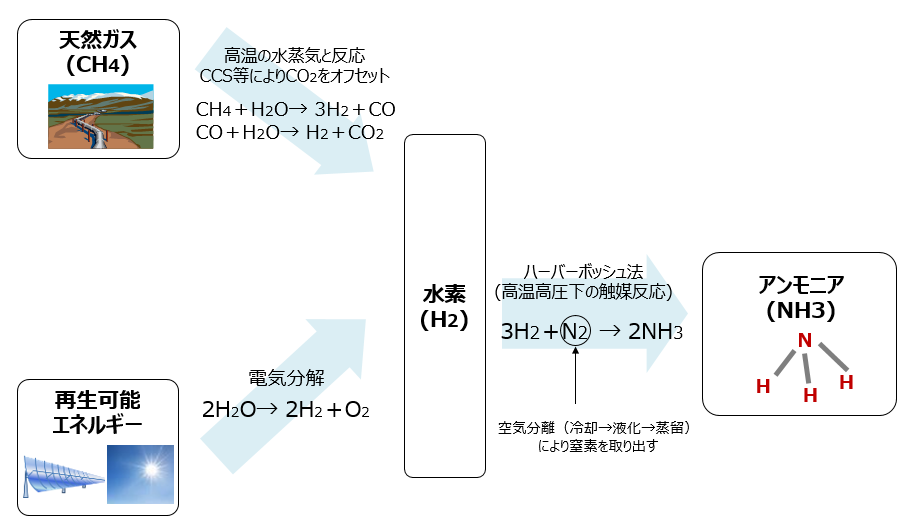



アンモニアが 燃料 になる 前編 身近だけど実は知らないアンモニアの利用先 スペシャルコンテンツ 資源エネルギー庁




Lihat Cara Penyelesaian Di Qanda




アクセス化学 例題解説 基本例題90 銅イオンの反応




金属イオンの分離実験の語呂合わせ 17h29大学入学共通テスト試行調査第1回第2問 問2 A B 入試化学を語呂合わせで解く大学入試ゴロ化学



塩酸とアンモニアが完全に中和するときの化学反応式を書けという問題についてな Yahoo 知恵袋



Matsuyamakita H Esnet Ed Jp Wysiwyg File Download 1 2868




アンモニア水とテトラアンミン亜鉛 の化学式についてですが なぜアンモニアは4mo Clear
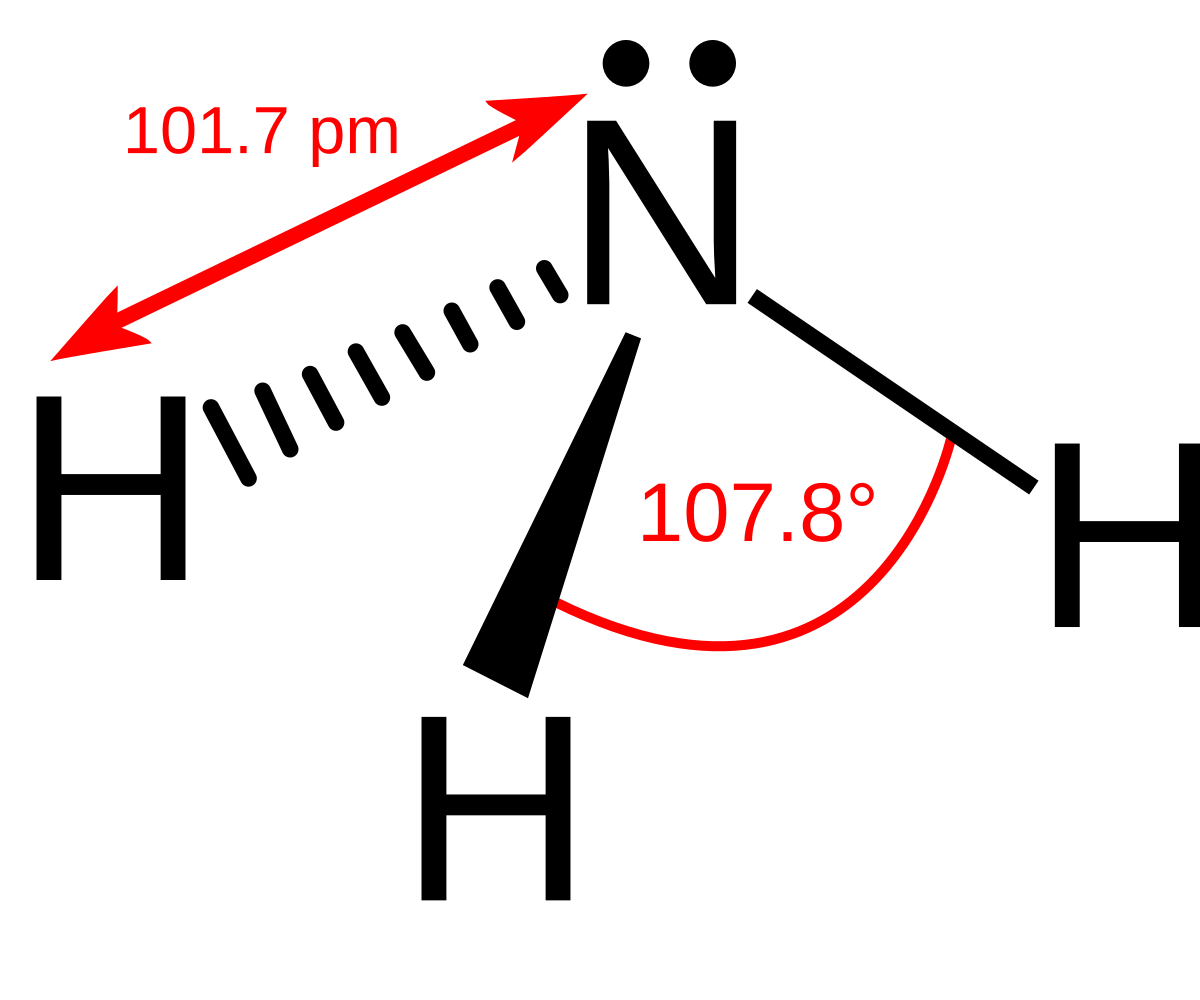



アンモニア Wikipedia




氷やアンモニア水は単体 純物質 化合物 混合物
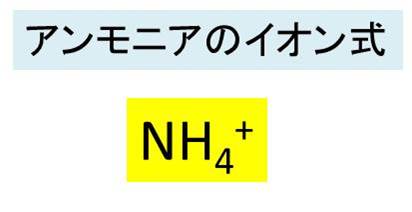



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は



化学実験 Ii属 銅



化学の質問です 酸化銀にアンモニア水を加える時のイオン反応式を答 Yahoo 知恵袋




頻出 化学反応式 4 化学がちょっとだけ好きな社労士



化学実験 Iii属 アルミニウム




010 Mol Y L 500 Ml Mol Lihat Cara Penyelesaian Di Qanda




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット




中1 理科 化学 アンモニアの発生 12分 Youtube




頻出 化学反応式 16 化学がちょっとだけ好きな社労士



下線部の反応はスルホ基を持つ化合物に濃アンモニア水を加えた反応です Yahoo 知恵袋




アンモニアを含んだ排水の処理 水処理に関するご相談は 栗田工業
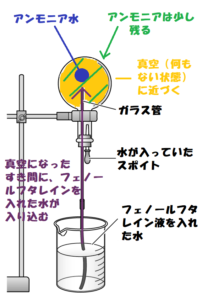



アンモニアの性質まとめ 中学生用



炭酸アンモニウム Wikipedia




尿素scrシステムについて アドブルーと同等品質の尿素水なら低価格のオプティ エコツーライト



Www Yone Yama Co Jp Shiyaku Msds Pdfdata 1275s Pdf
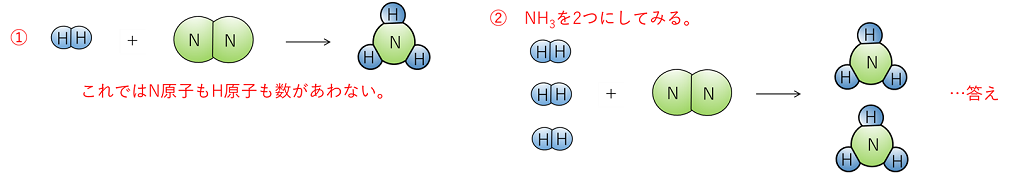



化学反応式
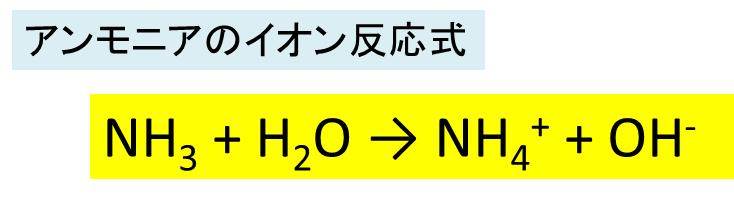



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は



第57章 実験 鉄イオン



気体に関する化学変化




完全版 入試に出るアンモニアの製法をまとめたった 化学受験テクニック塾




Album




沖縄県名護市立名護中学校 理科 酸 アルカリと塩 化学変化とイオン 松田 晋介教諭




どうしてアンモニアの価数は3では無いのですか Clear



化学実験 Iv属 コバルト



化学反応式
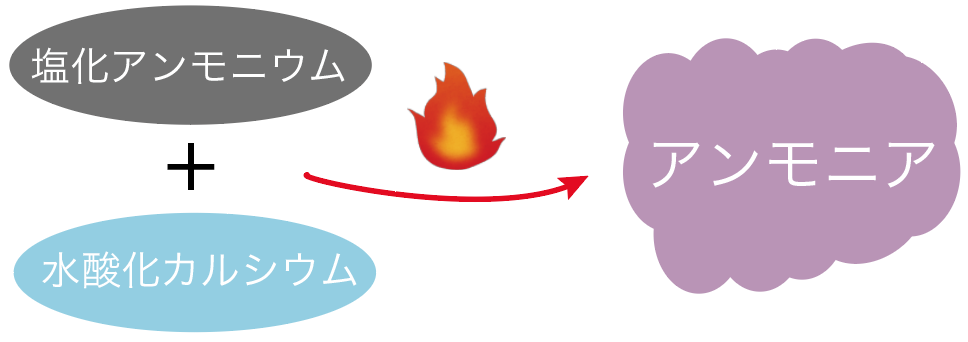



中1理科 3分でわかる アンモニアの発生方法 作り方 集め方 性質 Qikeru 学びを楽しくわかりやすく




質問です Clear




高校化学 アンモニアの製法 練習編 映像授業のtry It トライイット




混合物と純物質




水素 水 アンモニア メタンの化学式と分子モデル ベクトル図のイラスト素材 ベクタ Image




1 B 2 C 1 1 9 Descubre Como Resolverlo En Qanda
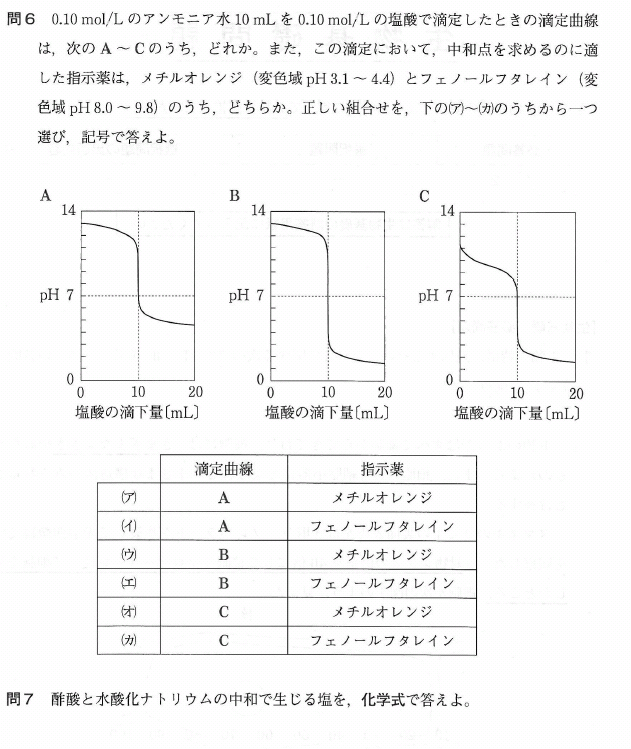



化学基礎模試解説 Kumonotaira




イオン式 電離式まとめ 中学理科 ポイントまとめと整理




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット



実験13 アンモニアの噴水 1年理科 化学 Takaの授業記録12



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理




Album




授業に潜入 おもしろ学問 自然科学科目群 化学 化学概論 I 中村敏浩 教授 京都大学広報誌 紅萠
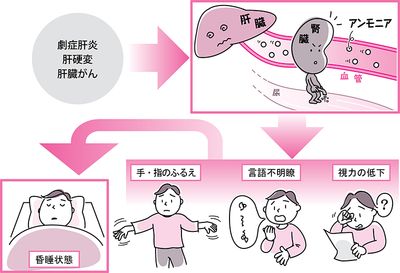



アンモニアとは コトバンク




なぜ中和で水を生じない場合があるのですか Clear




理科とか苦手で 物質のすがた13 気体の発生と性質 4 アンモニア




実験8 9発熱反応 吸熱反応の導入について ラスカルのブログ




アンモニア水の電離式を写真のように誤解しています どうして紫下線のような式になるか教 Clear



実験 吸熱反応 2年理科 Takaの授業記録17



電離式の小テスト 3年理科 Takaの授業記録11



空気からパンを作る アンモニアの話 つくばサイエンスニュース




Zncl2にnh3を加えた時に起こる反応の化学反応式を書け もしnh3を過剰に加えた Clear




アンモニア Nh3 の電離式を教えてください Clear




See How To Solve It At Qanda
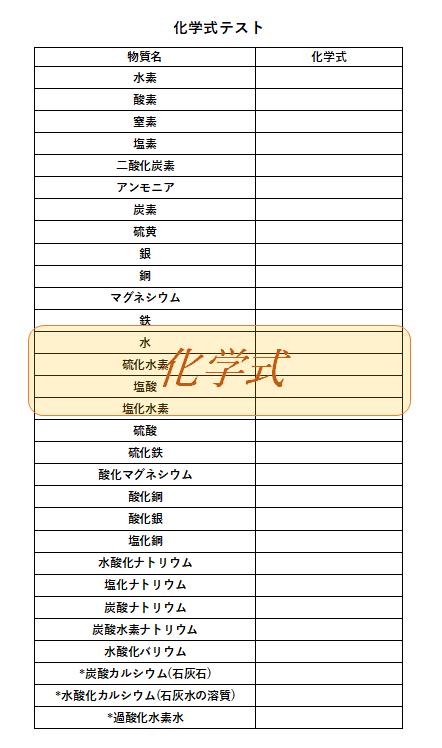



化学式記号 Tourotom1 1




頻出 化学反応式 16 化学がちょっとだけ好きな社労士



第55章 実験 アルミニウムと亜鉛




どうしてアンモニアだけ水を入れるんですか Clear



アンモニア 水 硝酸の化学反応式を教えてください アンモニアと水で硝酸は Yahoo 知恵袋



Http Www Keins City Kawasaki Jp 9 Ke9104 Jikken 30 Pdf




高校化学 アンモニアと沈殿 映像授業のtry It トライイット



1



3




1 Lihat Cara Penyelesaian Di Qanda



化学の質問です 2番と3番はどちらも大量のアンモニア水を塩化銀 酸化銀 Yahoo 知恵袋
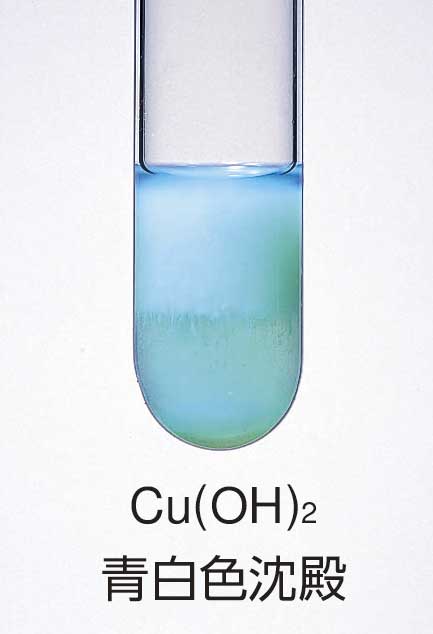



アクセス化学 例題解説 基本例題90 銅イオンの反応




高校化学 塩化アンモニウムの加水分解 映像授業のtry It トライイット




6 1 酸と塩基 おのれー Note




理科 中2 7 化学反応式の作り方 Youtube



2 o 問1 次の各化学反応式に係数を入れよ



2章a 類題1 4 0004 Top A 問題 次の各問いに答えなさい 問1 Cu2 と Fe3 を含む混合水溶液がある この2つの陽イオンを分離するために次の水溶液を使用した どちらが適切ですか 反応式を書いて説明しなさい 1 水酸化ナトリウム水溶液 2 アンモニア水
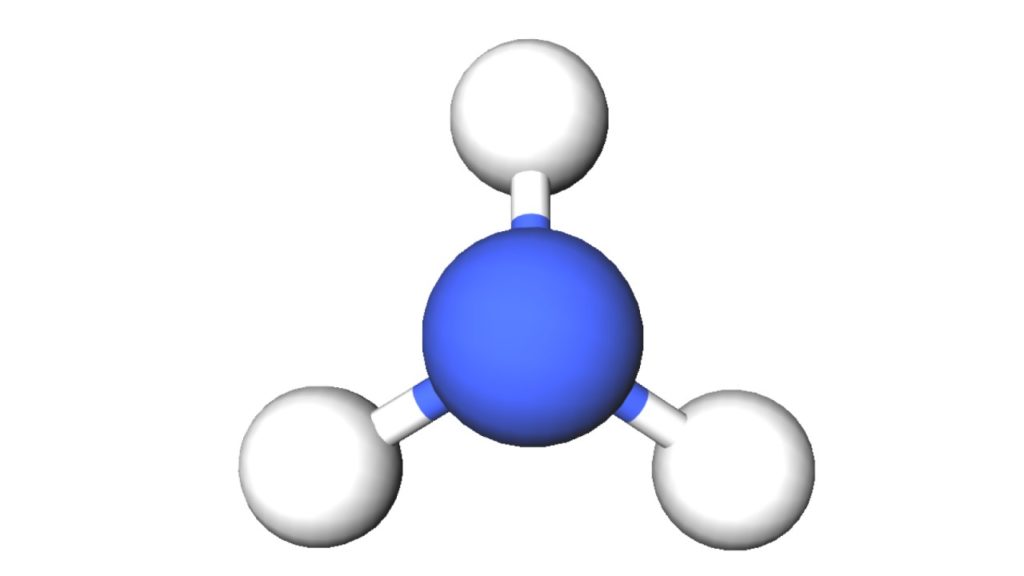



アンモニアはなぜアルカリ性を示すのか アンモニアの特徴とともにわかりやすく解説 ジグザグ科学 Com




アンモニアと塩化水素の中和反応 化学がちょっとだけ好きな社労士
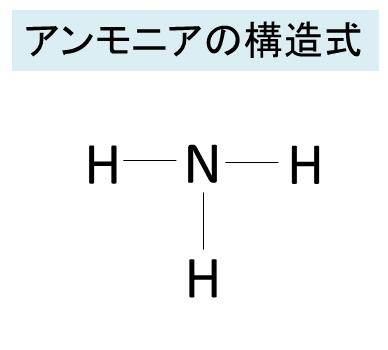



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は




高校化学基礎 塩基の価数 映像授業のtry It トライイット
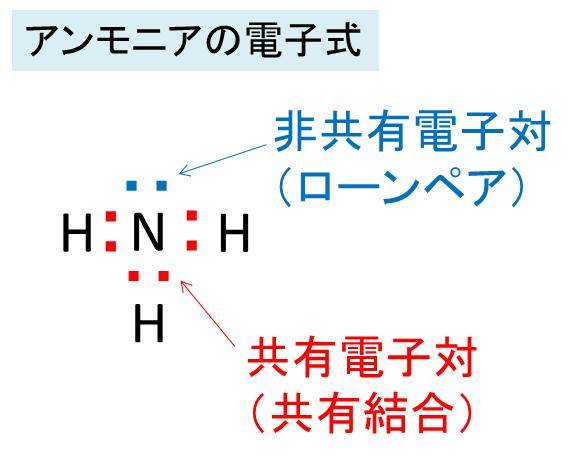



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は




3分でわかるアンモニアの発生方法 中学理科のすゝめ 定期考査対策から受験まで



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理




銀が溶けた溶液に少量のアンモニア水を加えた時のイオン反応式をかけ 化学 教えて Goo



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Inorganic How To Make Nh3




汚れとお掃除の百科事典 ナチュラルクリーニング アンモニア水 サニクリーン



0 件のコメント:
コメントを投稿